
Les recherches présentées dans ce chapitre sont une illustration de la richesse et de la diversité des travaux scientifiques menés au sein de l’institution ; elles ne constituent nullement une liste exhaustive.
Le groupe du Prof. Michel Gilliet du Service de dermatologie et vénéréologie a identifié une nouvelle fonction de la cytokine IL-26 présente dans la peau atteinte de psoriasis. Cette découverte a été publiée dans Nature Immunology.
L’équipe de recherche a démontré que l’IL-26 peut agir de façon indépendante de son récepteur ; en tant que protéine antibiotique, elle est capable de tuer directement les microbes envahisseurs et de déclencher une inflammation en se liant à l’ADN issu des microbes détruits ou des cellules endommagées de l’hôte.
Des anticorps pouvant bloquer la fonction inflammatoire de la cytokine IL-26 ont été identifiés. Les résultats préliminaires d’une neutralisation de l’IL-26 dans des modèles précliniques de psoriasis sont encourageants. Cette approche pourrait donner lieu à une application clinique pour le traitement de cette maladie.
Etant donné l’association faite entre l’IL-26 et d’autres maladies inflammatoires comme la maladie de Crohn, l’arthrite rhumatoïde et la sclérose en plaques, cette découverte pourrait avoir d’importantes répercussions au-delà des pathologies cutanées.Cette découverte a été publiée dans la revue Nature Communications par la chercheuse Annette Ives, la Prof. Nathalie Busso, directrice du Laboratoire de rhumatologie, et le Prof. Alexander So, chef du Service de rhumatologie et du Département de l’appareil locomoteur. Elle ouvre la voie au développement de nouveaux médicaments.
En bloquant la xanthine oxidase ainsi que la production de radicaux libres (molécules chimiques instables produites en faible quantité par l’organisme) générés par cette enzyme, il serait possible d’agir sur l’inflammation, par exemple dans les cas de maladies vasculaires et auto-inflammatoires. Cette stratégie, qui commence à être testée sur des modèles animaux, ouvre de nombreuses perspectives.L’intestin grêle est le principal site d’absorption des nutriments. Le bol alimentaire y est digéré et transporté vers les vaisseaux sanguins et lymphatiques. Plus précisément, les acides aminés et les glucides sont transportés directement par les vaisseaux sanguins intestinaux, alors que les acides gras sont absorbés par des capillaires lymphatiques hautement spécialisés: les lactifères.
Bien que le passage des lipides via les lactifères soit connu depuis longtemps, les mécanismes moléculaires régulant ce processus sont encore largement méconnus. Souvent oubliés, les vaisseaux lymphatiques intestinaux jouent un rôle majeur dans le corps humain.

Jeremiah Bernier-Latmani, post-doctorant au laboratoire de la Prof. Tatiana Petrova au sein du Département d’oncologie UNIL-CHUV, a développé une nouvelle technique d’imagerie 3D permettant de prendre des images très précises de l’intestin grêle. Grâce à cette technique, il a été possible de constater que les lactifères, contrairement aux autres vaisseaux lymphatiques, ont une prolifération augmentée, suggérant un renouvellement constant.
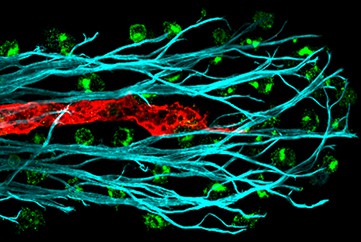 Image 3D en immunofluorescence des vaisseaux lymphatiques intestinaux dans l’intestin grêle de souris. © Dr Jeremiah Bernier-Latmani, UNIL-CHUV.
Image 3D en immunofluorescence des vaisseaux lymphatiques intestinaux dans l’intestin grêle de souris. © Dr Jeremiah Bernier-Latmani, UNIL-CHUV. En novembre 2015, cette étude a fait l’objet d’une publication dans l’édition en ligne du Journal of Clinical Investigation ainsi que d’un Research Highlights dans Nature Reviews Gastroenterology & Hepatology.
En décembre 2014, un vaccin candidat contre le virus Ebola était testé à Lausanne sur 120 volontaires en bonne santé.

L'essai clinique du ChAd3-EBO-Z, développé par les laboratoires GSK et les instituts nationaux de santé américains, était dirigé par le Prof. Blaise Genton, chef du Centre de vaccination et médecine des voyages de la Policlinique médicale universitaire.
Pendant plusieurs mois, les observations sur les volontaires ont été transmises au jour le jour à l’Organisation mondiale de la santé (OMS) et aux parties prenantes de la lutte contre l’épidémie. Ces données ont montré que le vaccin ne provoquait pas d’effets indésirables imprévus et qu’il induisait des réponses immunes significatives, mais dont l’amplitude était probablement insuffisante pour espérer une protection maximale.
Ces observations ont permis à l’OMS de poursuivre des études d’efficacité avec des doses plus fortes au Liberia et en Guinée. Cela a grandement accéléré le développement du vaccin candidat.
Menée en un temps record grâce notamment au financement de 1,7 million octroyé par la Confédération dans le cadre du programme Horizon 2020, cette étude a été publiée en décembre 2015 dans la revue The Lancet Infectious Diseases.
Communiqué de presse: Vaccin contre le virus Ebola: les résultats prometteurs de l’étude menée à Lausanne sont publiés par le CHUV et la PMU (PDF)
Une collaboration entre les groupes de recherche des Prof. Takao Hensch de l’Université de Harvard et Kim Do Cuénod du Centre de neurosciences psychiatriques a été publiée en janvier 2015 dans la revue Biological Psychiatry. Les scientifiques y exposent un nouveau concept susceptible d’expliquer l’apparition de la schizophrénie.

L’apparition de la schizophrénie serait liée à une perturbation des périodes critiques lors du développement du cerveau. Durant ces périodes, les connexions nerveuses du cerveau sont modifiées de manière permanente par le vécu du sujet. Un type de neurones inhibiteurs dits « à parvalbumine » en régule le déclenchement et la fin. La formation de myéline, gaine qui protège les fibres nerveuses, est également liée à la fermeture d’un cycle.
Or la dérégulation des oxydations du cerveau, dont la Prof. Kim Do Cuénod a démontré l’implication dans la schizophrénie, entrave le développement des neurones à parvalbumine et la formation de la myéline. Ainsi pourrait se créer un décalage ou une fermeture incomplète des périodes critiques, ce qui entraînerait une plasticité synaptique altérée et par conséquent les désorganisations que l’on observe chez les patientes et patients atteints de cette maladie.Des expériences chez la souris ont montré que le stress oxydatif empêche la maturation des neurones à parvalbumine et retarde la fermeture de la période critique pour le système visuel. En spéculant, on pourrait généraliser cette observation à d’autres domaines sensoriels, cognitifs, affectifs ou sociaux. De telles prolongations des périodes critiques ouvriraient la voie à des interventions cognitives visant l’amélioration de la plasticité synaptique et la prévention des troubles schizophréniques.
Ce nouveau concept a été élaboré dans un article de revue publié en 2015 dans Schizophrenia Bulletin.
La dégénérescence maculaire de type humide est la principale cause de la perte de la vue chez les personnes âgées.

Elle survient lorsqu’un fluide s’accumule anormalement sous ou dans la rétine. Une nouvelle étude publiée dans The American Journal of Pathology par Yvonne de Kozak et Francine Behar-Cohen, directrice de l’Hôpital ophtalmique Jules-Gonin, explique pour la première fois une des causes de cette maladie et offre de nouvelles méthodes de traitement.
L’étude en question suggère que l’exposition répétée à des stimuli, comme des allergènes ou des agents infectieux, peut conduire les mastocytes, des globules blancs circulant dans le sang sous forme immature, à libérer leur contenu de manière répétée. Ce processus, nommé dégranulation, pourrait entraîner la rupture des barrières hémato-oculaires et l’accumulation de liquide sous-rétinien. Grâce à un modèle animal dans lequel la dégranulation mastocytaire avait été induite chimiquement, les chercheurs ont pu tester que l’administration préalable d’une substance qui bloque la libération des médiateurs inflammatoires entraînait une diminution des cas de décollement de rétine. L’inhibition pharmacologique de la dégranulation mastocytaire pourrait donc avoir un potentiel thérapeutique important.Les traitements immunosuppresseurs ont permis d’améliorer considérablement la survie des receveurs d’organes. Ces traitements « antirejet » favorisent cependant la survenue d’infections, comme l’aspergillose invasive causée par le champignon Aspergillus. On ignore pourquoi certains greffés développent une aspergillose, alors que d’autres, pourtant exposés à des risques similaires, y échappent. Il est donc difficile d’identifier les individus qui pourraient bénéficier d’un traitement préventif.
La Dre Agnieszka Wójtowicz, biologiste dans le groupe du Dr Pierre-Yves Bochud au Service des maladies infectieuses, a montré que la susceptibilité à l’aspergillose invasive chez les receveurs d’organes solides est associée à un polymorphisme du gène de la protéine « long pentraxine 3 » (PTX3). Celui-ci entraîne un recrutement insuffisant de cellules immunitaires (granulocytes neutrophiles) au site d’infection. On sait par ailleurs que chez les receveurs de greffes de moelle, c’est le polymorphisme PTX3 du donneur, et non celui du receveur, qui génère une susceptibilité accrue à l’infection.
Bien que l’exploration du génome humain connaisse un développement extraordinaire, il existe encore peu d’applications dans la pratique médicale. Le polymorphisme PTX3 constitue désormais un des marqueurs les plus prometteurs dans le domaine de l’immunogénétique des infections. Cette étude est parue dans la revue Clinical Infectious Diseases.

Cette ligne de recherche menée en collaboration par le Service des maladies infectieuses, le Centre de transplantation d’organe et la Swiss Transplantation Cohort Study a été récompensée par le Prix du meilleur poster lors du Congrès annuel de la Société suisse de transplantation en 2016 (Dre A. Wójtowicz), par le Clinical Science Award à ce même Congrès en 2015 (Dr Oriol Manuel et Pierre-Yves Bochud), et par le Prix du meilleur poster aux journées du Département de médecine (Dre A. Wójtowicz). Le CHUV est l’un des acteurs principaux de la STCS depuis ses débuts en 2007.